こんにちは、カヲルです!
今回は熱力学(Thermodynamics)を扱いたいと思います。
熱力学は産業革命の原動力となった蒸気機関の実用化と性能向上への取り組みから発展してきた歴史がありますが、現在のものづくりでも非常に重要な学問となっています。
熱力学の応用範囲は非常に広く、エンジン、ポンプから材料の開発まで幅広く活用されていますので、是非見ていってもらえればと思います。
熱と仕事

温度と熱
「熱」と聞いてまず思い浮かべるのは風邪を引いたときに「熱が出た」という使い方ではないでしょうか。
これは日常生活で使う言葉としては正しいですが、物理の言葉としては正しくありません。
正しくは「温度が上がった」と言うことになります。
温度(Temperature)は簡単に言うと物体の温かさや冷たさを示す指標となります。
熱力学の世界では絶対温度を用い、単位はK(ケルビン)になります。摂氏温度との関係は下記になります。
[絶対温度(K)]=[摂氏温度(℃)]+ 273.15

絶対温度は熱力学温度やケルビン温度とも言ったりもするよ。
摂氏温度は1気圧で水が凍る温度を0 ℃とし、沸騰する温度を100 ℃としますが、絶対温度は温度の下限値を0 Kとするよ。(マイナスはない)
では次に熱(Heat)とはなんでしょうか。これを考えるために例として入れたてのホットコーヒーを部屋の中に置いておくシチュエーションを考えます。
最初はコーヒーは温かいですが、放っておくと冷えてしまいます。
これは温度が高い物体(コーヒー)から温度が低い物体(周りの空気)へ何かが移動したものと推測できます。その何かを熱と呼んでいます。
なお熱の単位はJ(ジュール)となります。
仕事
熱力学は熱と仕事(Work)を扱う学問になります。仕事には下記のものがあります。
力学的仕事
力学的仕事はピストン付きのシリンダに封入された気体へする仕事などが挙げられます。本記事は機械設計への応用を想定しているため、力学的仕事(体積仕事)を中心とします。
電気的仕事
電池や電気分解などを考えるときに、化学反応の進行にともなって外部回路を移動する電子の仕事を扱う場合もあります。
表面仕事
界面化学を考えるときに、表面張力による仕事を考える場合もあります。
では実際に力学的仕事について考えていきましょう。
まず、下図のようにシリンダとピストンで構成される密閉空間での仕事を考えます。
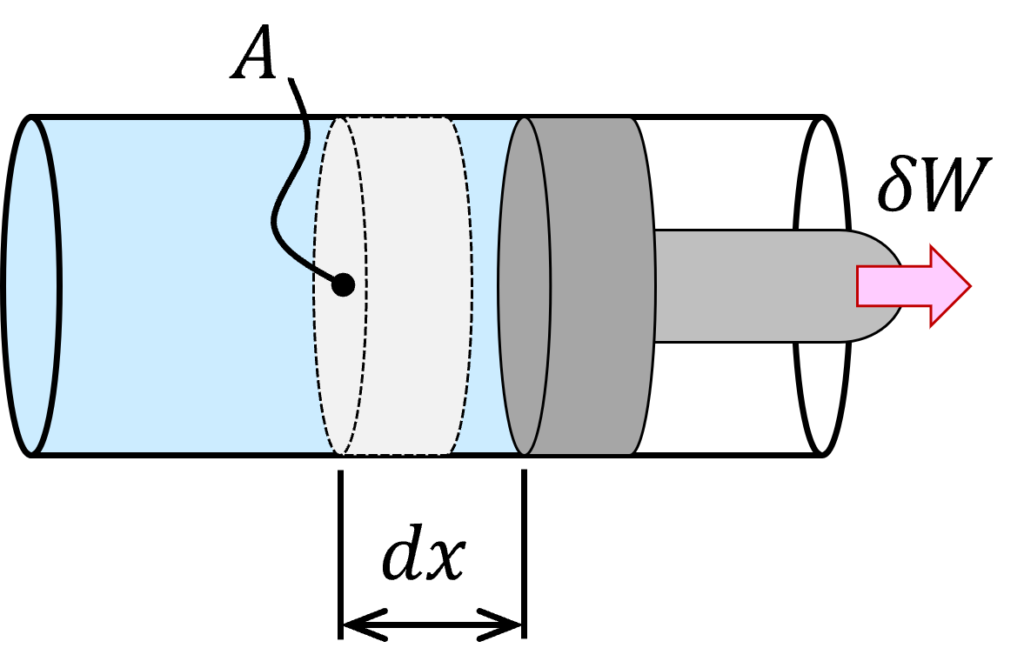
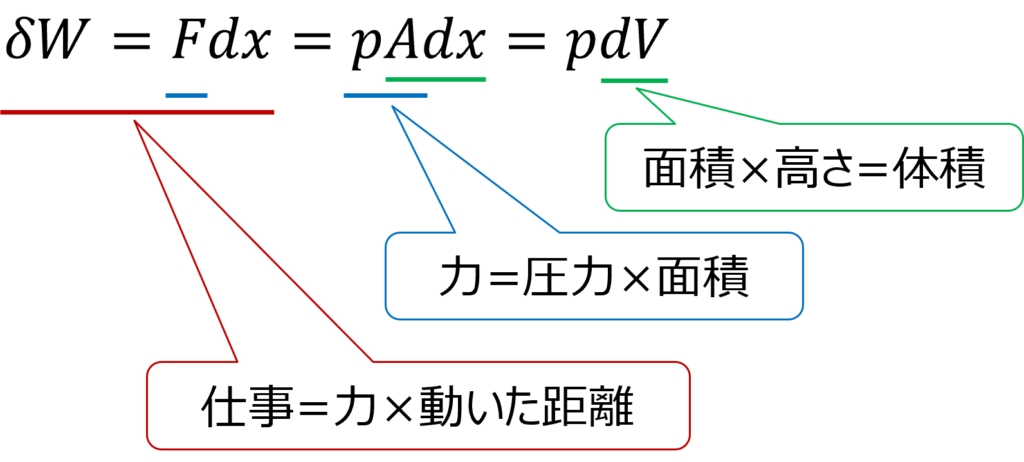
気体の圧力をp、体積をV、ピストンの断面積をA とし、ピストンが微小距離dx 動いたとするとこの過程でなされた仕事δW は下式となります。
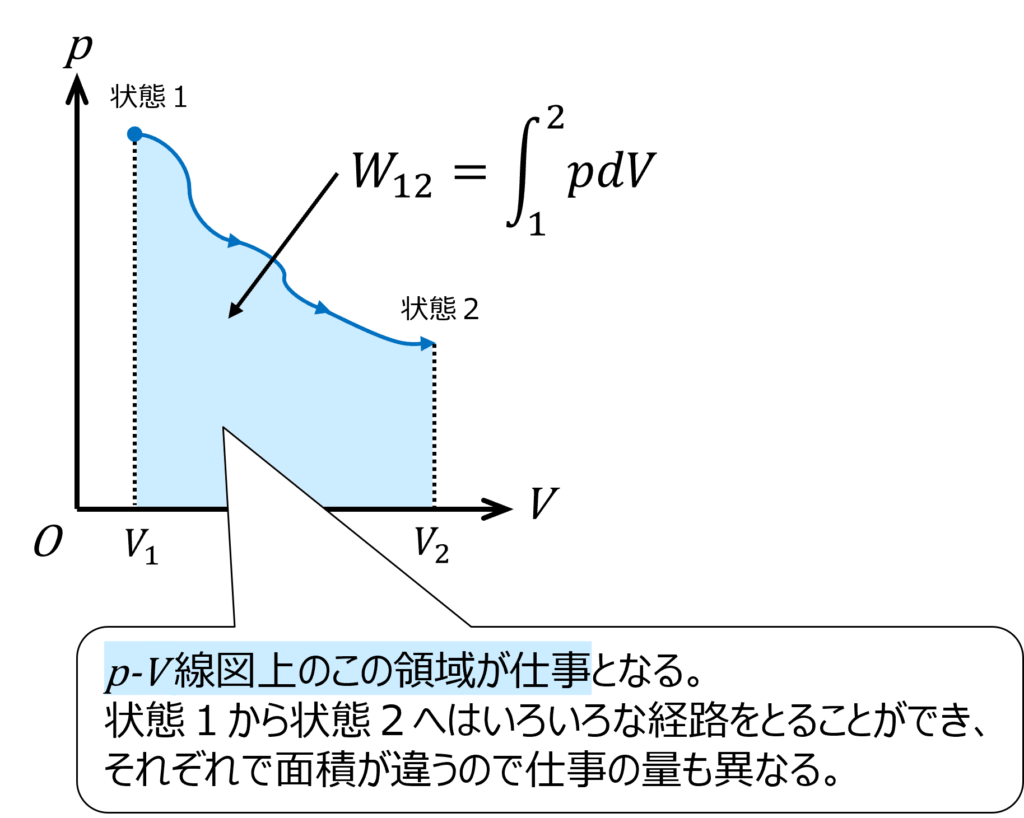
実際のピストンの移動はdx より大きく、状態1から状態2への仕事W12 を考えると変化は微小ではないので、系内の圧力p は状態変化の間に変化することも考える必要があります。
前頁まではシリンダとピストンで構成されるモデルで考えましたが、より一般的な問題として下図のような体積仕事を扱ってみます。
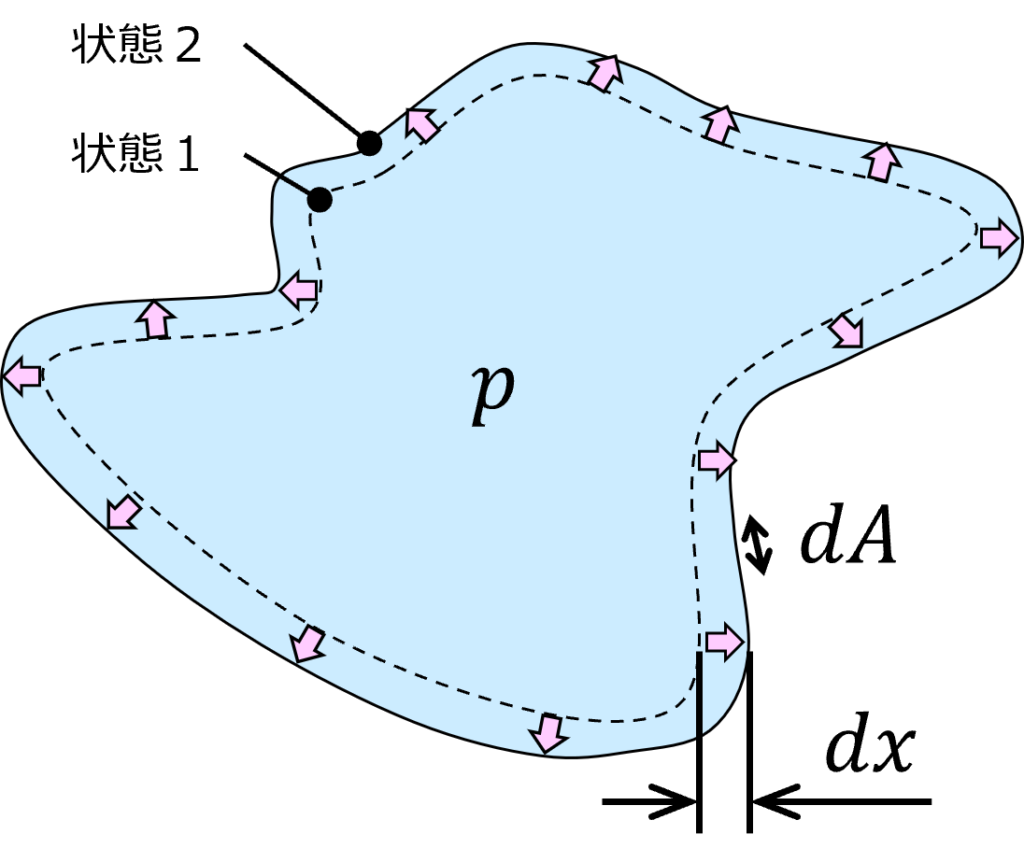
このとき、状態1から状態2への仕事W12 は下式のように表現できます。
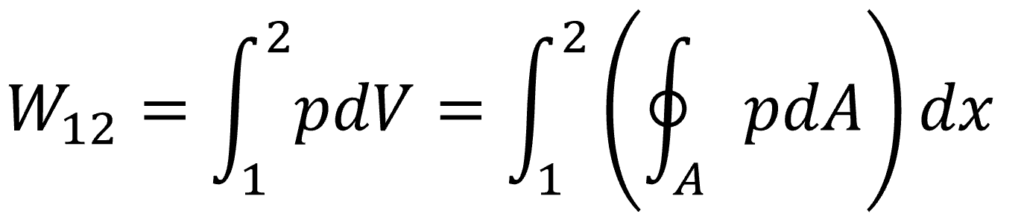

∲(線積分)を忘れちゃった方は下記を見てね!
次に下図のように状態1から状態2の間をサイクルで作動する場合の正味仕事Wnet(net work)を考えます。

- 1-A-2は膨張過程であり、系が周囲にする仕事になります。
- 2ーB-1は圧縮過程であり、周囲から系がする仕事になります。
よって、1サイクルの間に系が周囲にする仕事は下式で表すことができます。
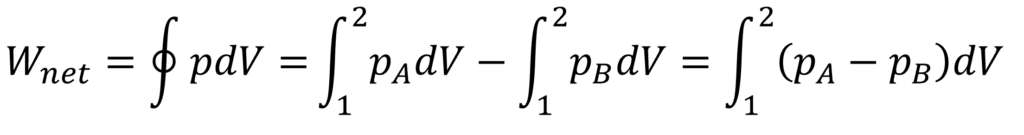

熱力学では対象とする範囲を系(System)と言い、系の外側を周囲(Surroundings)というよ!
【参考】系の種類
系には孤立系、閉じた系、開いた系の3つがあります。
孤立系(Isolated system)
周囲と物質のやり取りがなく、エネルギーのやり取りもない系を言います。
閉じた系(Closed system)
周囲と物質のやり取りはないが、エネルギーのやり取りは行われる系を言います。
開いた系(Open system)
周囲と物質のやり取りもエネルギーのやり取りも行われる系を言います。
熱力学第一法則

熱力学第一法則(エネルギー保存則)
熱力学第一法則(the first law of thermodynamics)は「熱と仕事はともにエネルギーの1形態で、仕事はエネルギーに変えることが可能で、またその逆も可能である」と表現されます。

体積、圧力、温度、内部エネルギーなどは最初と最後の状態が定まれば求めることができる量であり状態量(quantity of state)と呼ばれるよ。
これに対して、熱や仕事は最初と最後の状態だけでは求められない量のため状態量ではないよ。(積分する経路によって値が変わるよ)
これは熱が力学的仕事を含むエネルギーの1形態としているため、エネルギー保存則(energy conservation low)に対応して解釈することができます。
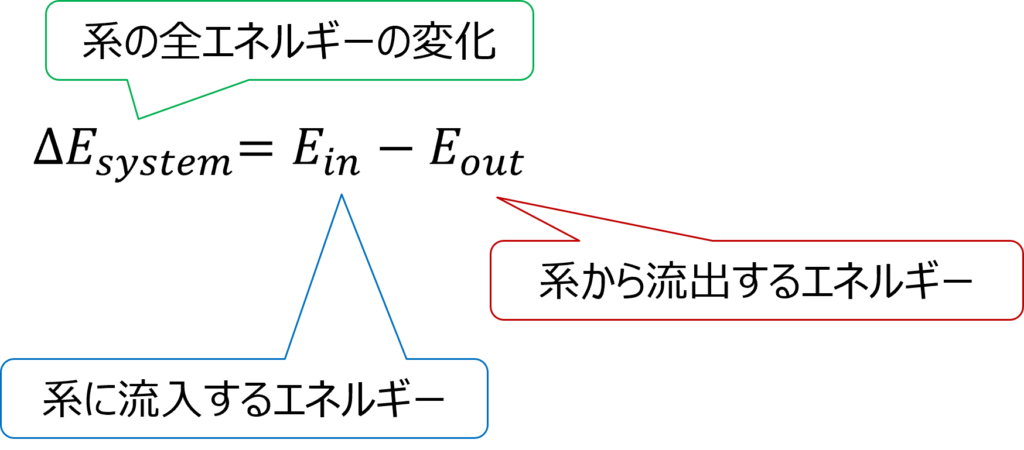

エネルギー保存則は外とエネルギーがやり取りされない限りエネルギーは変化しない(勝手に増えたり減ったりしない)という法則だね。
閉じた系は周囲と熱や仕事のやり取りがある場合があります。
エネルギー保存則より系が保有するエネルギーは、このやり取りしたエネルギー量だけ増減することになります。
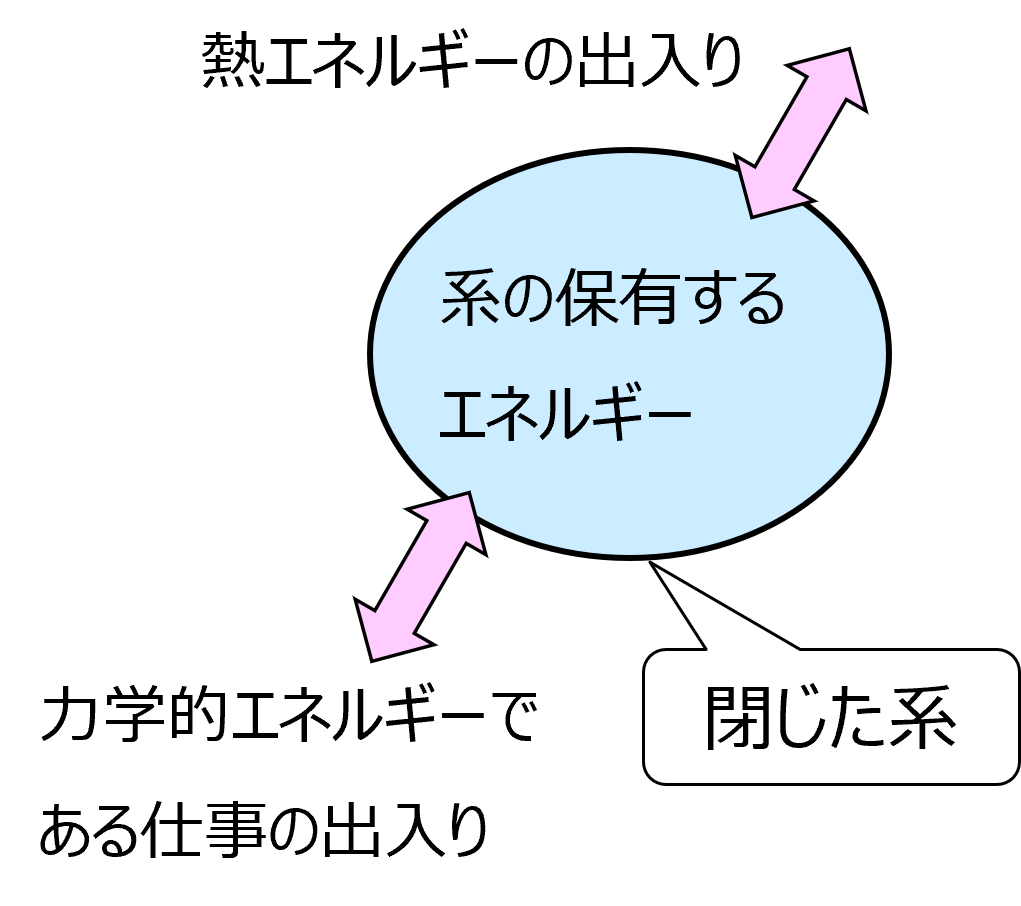
ここで、系全体の巨視的な動きによる運動エネルギーEK、重力によるポテンシャルエネルギーEP、分子のもつ巨視的にみて方向性のない微視的なエネルギーである内部エネルギーU の和が系が保有するエネルギーになります。
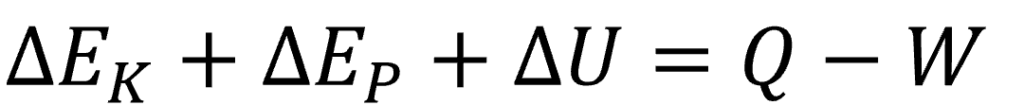
通常は系は静止している(ΔEK = 0, ΔEP = 0)か内部エネルギーに対して十分小さいので
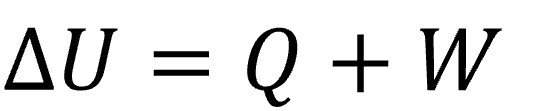
となり、この形が一般的な熱力学第一法則の式になります。

内部エネルギーに関しては高校物理で習う気体分子運動論(kinetic theory of gases)も復習してみてね!




